Oggi parliamo di terapia genica, con un particolare occhio di interesse rivolto verso la branca oculare di questo tipologia di terapia, nel dettaglio parliamo di quanto avvenuto presso il Policlinico Vanvitelli di Napoli, ove l’innovativa terapia genica oculare è stata utilizzata per trattare due bambini affetti da amaurosi di Leber, una patologia congenita responsabile di cecità infantile, con grande obbiettivo quello di restituire la vista a chi ne affetto, difficile però da raggiungere.
La patologia
L’Amaurosi congenita di Leber è una patologia genetica a carattere autosomico recessivo che negli anni porta ad una forte ipovisione che progredisce poi nel tempo ad una cecità completa, essa è accompagnata spesso anche da un movimento oculare continuo e involontario, noto come nistagmo.
La tipologia di trasmissione su cui si basa la malattia richiede la presenza di due genitori portatori di un gene malfunzionante, che nel caso di omozigosi nel figlio porta allo sviluppo della sindrome propriamente detta, con i genitori invece portatori sani, la diagnosi si basa sull’elettroretinogramma, che serve a valutare la funzionalità dei fotorecettori, accostata ad analisi genetiche.
L’incidenza della malattia varia da 1,25 a 3 casi ogni 100.000 bambini all’anno, i difetti genetici che portano all’esordio di malattia, sono delle mutazioni nei geni che codificano proteine specifiche della retina, tra i quali: GUCY2D (17p13.1), CEP290 (12q21.33), RPGRIP1 (14q11.2), RDH12 (14q24.1), SPATA7 (14q31.3), AIPL1 (17p13.1), RD3 (1q32.3), CRB1 (1q31-q32.1), CRX (19q13.3), IMPDH1 (7q31.3-q32), IQCB1 (3q21.1), KCNJ13 (2q37), LCA5 (6q14), NMNAT1 (1p36.22), e TULP1 (6p21.3).
Tali mutazioni portano ad un deficit funzionale o ad una distrofia retinica, con lo specifico caso di CRX e IMPDH1 che porta ad un esordio precoce di malattia con una progressione più rapida e infausta rispetto alle altre.
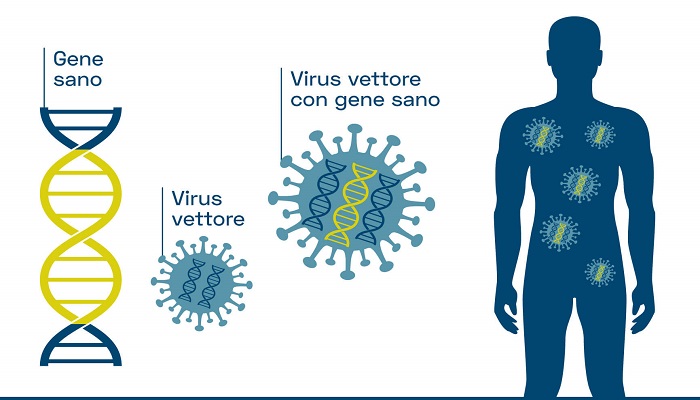
Presso l’istituto napoletano è stata attuata una nuova terapia basata appunto sulla possibilità di inserire il gene funzionante al posto di quello difettoso, parliamo appunto della terapia genica nella sua più recente tecnica CRISPR-Cas9 , la quale si avvale di un vettore virale come trasportatore del materiale genetico terapeutico, i vettori sono vari: adenovirus, virus adeno-associati e retrovirus, che in questo caso hanno trasportato il Sepofarsen, che agisce legandosi all’RNA CEP290 mutato per consentire il corretto splicing.
La somministrazione è stata intravitreale ed è stata molto rapida e anche tranquilla, grazie ad un’anestesia topica mediante colliri appositi, la bambina sta bene e anzi, nonostante il lungo percorso riabilitativo che l’aspetta, la malattia non è progredita e sono già stati evidenti i primi miglioramenti.













